

甲状腺髓样癌(MTC)是一种起源于甲状腺滤泡旁细胞(C细胞)的神经内分泌恶性肿瘤,临床上较为罕见,发病率仅占所有甲状腺癌的3-5%,但在甲状腺癌相关死亡中的占比高达15%。
过去10余年间,晚期MTC从无药可治的窘境迎来两次飞跃性进展。首先,多靶点酪氨酸激酶抑制剂凡他尼布、卡博替尼、安罗替尼相继在美国或中国大陆获批,为这部分患者带来了曙光。其次,近两年来,高选择性RET抑制剂塞尔帕替尼[2]和普拉替尼[3]治疗RET变异型晚期甲状腺癌(入组患者绝大部分是MTC)的临床试验取得成功,并获得FDA加速批准,进一步丰富了治疗选择。
然而从整体上看,晚期MTC患者仍然面临着适应证受限,药物毒性强,以及较高的耐药风险等问题,并且仍然缺乏有效的多线治疗模式,故迫切需要更为精准的治疗策略。
与分化型甲状腺癌相比,MTC具有更高的遗传倾向及复发转移潜能,并且在临床表现、预后、诊断、治疗等多个方面存在显著差异,综合分析MTC从基因型到表型的异质性有助于深入理解此疾病。
近日,复旦大学附属肿瘤医院头颈外科嵇庆海教授、王宇教授、魏文俊副主任医师与西湖大学郭天南教授合作,在Cell Discovery上发表重要研究成果。复旦大学附属肿瘤医院头颈外科与西湖大学合作,联合浙江省肿瘤医院、常州市第二人民医院、泰州市人民医院、北京大学深圳医院等国内多个中心,收集了102例MTC肿瘤及配对样本建立队列,并进行了全外显子组、转录组、甲基化组、常规蛋白组和磷酸化蛋白组测序。
基于以上测序数据,他们发现了新的MTC致病基因,绘制了国际上首个甲状腺髓样癌蛋白基因组学全景图谱(亦是首个大体量样本的多组学文章)。此外,他们还提出了MTC“分子三分型”的概念,并对每种分子分型内部存在的多组学异质性展开深度探索,阐释潜在的精准治疗策略及方向。
在过往研究中,仅有50%-70%的MTC患者可以找到致病因素。在本研究中,研究人员利用目前世界上最大体量的MTC新鲜冻存组织样本队列,为超过91%的MTC患者找到了明确的致病基因,并且首次证实了BRAF和NF1基因在MTC致病过程中的驱动作用,丰富了MTC的驱动突变谱。
和既往认知一致的是,RET和RAS基因突变在该队列中占据主导作用,且存在显著互斥,但除了这两种经典癌基因之外,既往国际上尚未明确证实MTC中有其他驱动基因,尤其是重复突变基因。
在本研究中,研究人员在两个不伴任何其他驱动突变的散发性MTC病例中,分别检测到了BRAF非热点突变(p.G469A和p.T599dup,在其他神经内分泌肿瘤中已证实为驱动突变),并通过下游蛋白组学分析证实了两者存在不同程度的下游致癌通路激活。
另外,研究人员在该队列中发现了一个极为特殊的病例,这个患者除了MTC以外,还患有I型神经纤维瘤病,这种临床综合征目前仅有极少数报道,但具体病因尚未得到证实。
研究人员对这个患者样本进行了基因组、转录组、蛋白组联合分析后发现,该患者缺乏常见的MTC驱动基因突变(如RET、RAS等),但却伴有从胚胎卵裂过程中产生的NF1基因de novo截短突变(正常密码子提前变为终止密码子)。这个突变引发了NF1基因后续转录和翻译水平的剧烈下降,使得NF1这个重要的抑癌蛋白功能失活,进而导致了MTC和I型神经纤维瘤病。
通过上述分析,研究人员首次证实了NF1基因在MTC中的致病作用,进一步丰富了甲状腺髓样癌的驱动基因谱。
更为重要的是,研究人员对102个MTC肿瘤样本的蛋白组进行深入分析,将MTC分成蛋白表达异质性明显的三种分子分型:代谢型、基底型、间质型。
“代谢型”MTC患者中RAS基因突变显著富集,伴有多种糖代谢、脂代谢、蛋白代谢等多个代谢通路的活性增强。此外,“代谢型”肿瘤还具有MAPK和PI3K/Akt/mTOR通路激活、细胞周期激酶活性增强和基因组不稳定性(HRD评分)升高等特性,提示这部分患者可能从一些在研药物如MAPK/PI3K通路抑制剂、细胞周期抑制剂或PARP抑制剂中获益。
“基底型”患者则保留了更多MTC起源细胞(C细胞)的神经内分泌特性,相同体量的肿瘤组织,基底型肿瘤表达的降钙素、癌胚抗原(CEA)、嗜铬素、突触素等神经内分泌细胞标志物均显著增高。整体而言,基底型的肿瘤分化程度相对更高,预后最好,并且极少出现复发转移。因为这类肿瘤分型中癌胚抗原(CEA)的表达量远高于其他它两组,故目前已用于其他肿瘤临床试验的抗CEA抗体偶联药物值得在这一分型中做出进一步尝试。
相比前两种分型,“间质型”是恶性程度更高、侵袭性更强的一类肿瘤。在该分型中,恶性程度更高的RETM918T突变显著富集,并且绝大部分间质蛋白的表达都显著增高,尤其是与肿瘤转移密切相关的TNC蛋白表达水平更是其他分型的近3倍。
更为重要的是,这类肿瘤中血管生成相关蛋白VEGFR与PDGFR表达水平明显升高,它们是MTC已获批药物卡博替尼和安罗替尼最为重要的抗癌靶点,也是MTC在研药物索拉非尼、乐伐替尼、舒尼替尼等多种酪氨酸激酶抑制剂的靶点。此外,国产原研药物索凡替尼的靶点CSF1R也在间质型肿瘤中呈高表达状态,前期嵇庆海教授牵头的II期临床试验已证实,该药物对部分MTC患者有效[5]。以上结果表明,间质型肿瘤是以上几种获批或在研靶向药物最有希望的获益群体。
总的来说,本研究作为罕见肿瘤甲状腺髓样癌的首个真正意义上的大体量多组学研究,对甲状腺髓样癌蛋白基因组学全景图谱展开了详细描绘,发现该肿瘤新的驱动基因,提出了崭新的MTC分子分型,并且阐释了分子分型基础上的精准治疗策略,为后续机制挖掘、临床转化打下深厚基石,并提供了丰富的研究资源。


全国共有49家实验室报名参加,其中45家提交有效结果,仅23家通过评价活动,通过率为51.1%。

由中国临床肿瘤学会(CSCO)主办的"2020年中国临床肿瘤学年度进展研讨会"近日于线上顺利召开,会上专家学者们对2020CSCO消化道肿瘤指南更新做了总结,近几年颇受关注的免疫治疗在新版指南中地位突显,地位相较于旧版指南有所提升。
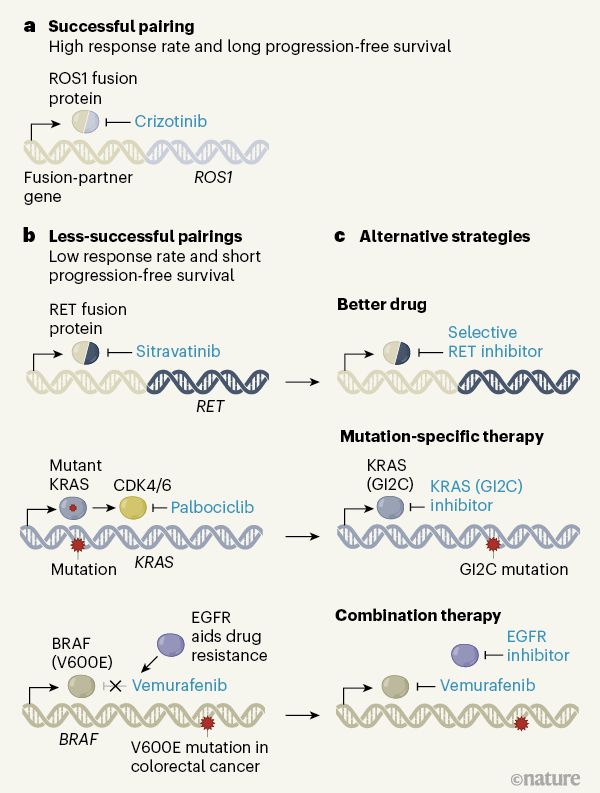
由伯明翰大学癌症研究中心英国临床试验小组领导的一项开拓性的肺癌研究强调了下一波精准医学研究,特别是治疗基因组复杂癌症需要考虑的重要因素。